hasáb alakot szokás adni (191. ábra). A két ellentett oldallap közöl az egyik a páros, a másik pedig a páratlan sorszámú forrasztásokat foglalja magába. A hasáb két oldalára erősített csavarok – az egyik az első bizmút-, a második pedig az utolsó antimon-rúddal közlekedvén – az oszlop áramvezetőit tartják.
Az élő állati test belső részeinek hőmérsékletét szintén kis thermoelektromos oszloppal határozzák meg, mely végeikkel összeforrasztott aczél és vörösréz tűkből van készítve.
A 194- és 195-dik ábrák közől az első egy thermo-elektromos elemet, a másik pedig az ilyen elemekből összeállított oszlopot tüntet elő,
4. Másodlagos áramok és elemek.
Láttuk, hogy az első galván-oszlopok áramát gyengítő okok egyike az volt, hogy másodrendű áramok mutatkoztak, melyek a fémlemezeken kiváló savas, alkalis, vagy gázalakú lerakódásokból eredtek. BECQUEREL kimutatta, mi módon lehet ez áramokat semlegesíteni az által, hogy az elembe a folyadékától likacsos fallal elkülönített második folyadék is tétetik, mely folyadék úgy van megválasztva, hogy az elektronegativ lemezen kiváló gázt vagy elemet elnyelje. Így keletkeztek a VI. fejezet 3. czikkében leírt állandó galván-oszlopok.
A másodrendű áramokat RITTER fedezte fel 1803-ban. Egy oszlop-alakú galván-láncz áramát egy másik oszlopon átvezetvén, mely csupán csak nedves posztóval elkülönített vörösréz-korongocskákból volt felépítve, azt vette észre, hogy ámbár ez utóbbi önmagában véve nem működött, az elsőnek hatása alatt áramot adott, mely az elsőével ellentett irányú. Igaz ugyan, hogy ez az áram gyenge és rövid tartamú volt. 1826-ban DE LA RIVE hasonlóan felismerte, hogy platina-lemezek között, melyeken vízbontás következtében oxygén és hidrogén váltak ki, szintén van ily másodrendű áram. A tünemény az elektródok polározódásának, s az áram maga polározódási áramnak neveztetik.
A másodrendű áramok ez idő óta sok fizikus vizsgálatának képezték tárgyát; közülök csak FARADAY, WHEATSTONE, POGGENDORFF, E. BECQUEREL, GAUGAIN neveit idézzük. E kérdés, kivált 1859 óta, midőn GASTON PLANTÉ, tudós franczia fizikus a különböző fémek és folyadékok befolyását a másod rendű áramok keletkezésére és intenzitására tanulmányozta, nagy fontosságra emelkedett. E fontosság mellett tanúskodnak azok a szép, tudományos és gyakorlati alkalmazások, melyek e fizikus vizsgálatainak következményei lettek. Vörösréz-, ezüst-, ón-, alumínium-, vas-, czink-, arany- és platina-elektródokkal ellátott voltaméterekkel kísérletezett, s mindegyiköknél a folyadékot is változtatta, melybe mártva voltak. Rájött, hogy valamennyi fém az oszlop positiv sarkán oxidálódván, az elsőrendű áram
266
megszakítása után támadt másodrendű áram annál erősebb, mennél teljesebb az oxidálás, feltéve azonban, hogy a keletkezett oxid a fémhez tapadva marad s a voltaméter savanyított folyadékában nem igen oldódik. Az oszlop oxidáló hatásának még az arany és ezüst sem állhattak ellen; bőséges oxid-réteggel vonódtak be és elég erélyes másodrendű áramot szolgáltattak. Igaz, hogy a platina látható módon nem oxidálódott, de az ellentett irányú másodlagos áram is rövidebb tartamú volt, mint azon fémeknél, melyek felületükhöz tapadó oxid-réteggel vonodtak be, s ez a hatás a voltameter positiv sarka körül képződő oxigénezett víznek rohamos szétbomlásából volt magyarázható. Másrészt a hidrogén hatása a platinával erősebb volt, mint bármely más fémmel, olyannyira, hogy az elektród, mely körül e gáz kivált, egy másik semleges elektróddal elég erős másodrendű áramot adott."
Ezen érdekes vizsgálatok legfontosabb eredménye azt fejezi ki, hogy a legerősebb másodrendű áram ólom-elektródos voltaméterből kap-
267
ható. Az ilyen voltaméternek elektromindító erejét az elsőrendű áram megszakítása után mérvén, azt találta PLANTÉ, hogy e es az erő másfélszer akkora – pontosabban 1,48–1,49 – mint a GROVE- vagy BUNSEN-féle, vagyis a legerősebb galván-elem elektromindító ereje."
Innét eredt az az eszméje, hogy másodrendű elemeket szerkeszt és azokat telepekké kapcsolja, úgy hogy ezáltal a galván-elemek munkáját akkumulálja vagy felhalmozza ugyanazon módon, a mint a statikai elektromosságot szokás szigetelő réteggel elkülönített nagyfelületű vezetőkön összesűríteni. PLANTÉ az ezen alapelven alapuló készülékeknek különböző alakokat adott. Az utolsót fogjuk leírni, melyben fokozatos tökéletesítések után megállapodott.

196. ábra. – A Planté-féle másodrendű telepnek egy eleme.
Két hosszú és széles ólomlemez, egymástól 5 milliméter vastagságú kaucsuk-szalagokkal elválasztva, tekercsalakba van összegöngyölítve és lemezkékben végződik, melyek az áramvezetők befogadására vannak rendelve. E tekercsek kis kaucsuk-keresztek közé vannak foglalva és azután hengeralakú üvegedénybe lebocsátva, mely 1/10-ed rész kénsavval savanyított vízzel van megtöltve. Keményített kaucsukból vágott fedő két fémdarabot hord, melyek a megtöltött elem másodrendű áramának zárására szolgálnak. Az elem két ólomlemezének kiálló végei G és H csiptetők segélyével (196. ábra) két kisebb BUNSEN-féle elemből összeállított oszlop sarkaival közlekednek, s ezenkívül M és M' rézlemezkékkel is. Ezek közöl az egyik A' csiptetővel állandóan közlekedik, a másik pedig P gomb és R vörösréz rugó útján az A csiptetővel bármikor közlekedésbe helyezhető. E csiptetők az E drótot tartják, melyen keresztül a másodrendű áramot átvezetni akarjuk.
Az ily módon összeállított másodrendű elem teljes erejét nem éri el mindjárt a kezdetben. Feltalálójának kifejezései szerint: formálásra, előkészítésre és edzésre szorul. "Midőn az új másodrendű elem, írja PLANTÉ, a galván-oszlop hatásának első ízben tétetik ki, csak rövid tartamú hatásokat ad. De ha az áramot több ízben vezetjük át, felváltva az egyik, azután a másik irányban és pedig elég hosszú időn át, hogy majd az egyik, majd a másik lemezen hiperoxid-réteg képződjék, közbe-közbe több napi nyugalmat engedvén az elemnek, hogy a lerakodásoknak idejök legyen összetartásra szert tenni, akkor a másodlagos hatások mind tartamban, mind pedig erősségben jelentékenyen öregbednek. Az ekként megfelelően formált,* edzett másodrendű elem, mely több órán keresz-
* Midőn egy másodrendű elem elegendően formaltnak tekinthető, több havi pihentetés nem hogy használna, mint a formálás műveleténél, hanem ellenkezőleg árt, mivel az elem ellenállását növeli és töltését hosszadalmasabbá és nehezebbé teszi. Előnyösebb tehát, ha időről-időre töltjük, vagy pedig egy gyenge oszlop segélyével állandóan töltve tartjuk, hogy a positiv lemezen a nem igen jól vezető kénsavas ólom képződésének eleje vétessék, mely az ólomhiperoxid lassú és önmagától végbemenő reductiójából ered." (GASTON PLANTÉ: Recherches sur l'electricité, Paris, 1879.)
268
tül az elsőrendű oszlop áramát magába fogadta s mely a nélkül, hogy az áramkör bezáratnék, magára van hagyatva, még egy sőt két hét elmúltával is oly áramot ad, mely elég erős arra, hogy 1/2 milliméternyi platinadrótot néhány pillanatig izzásban tartson. (6) [Elrontott hivatkozás!]
A most leírt ólom-elektródos másodrendű elemek megoldják a feladatot, mely valamely galván-forrás felesztette elektromosság felhalmozásában áll, – a veszteség 1/10-ed résznél nem több, – de ezek a forrásénál magasabb feszültséget adni nem bírnak. Ennek elérése végett PLANTÉ oly készülékeket szerkesztett, melyek segélyével a másodrendű elemek feszültségre kapcsolhatók össze. A 197-ik ábra 20 elemből összeállított telepet tüntet elő, melynel az elemek egy faállványban két sorba vannak felállítva; ennek felső részén CC' készülék látható, melynek segélyével az elemeket nagy felületre vagy nagy feszültségre lehet összekötni. Azonnal fogjuk látni, miért van a kommutátor a készülékhez kapcsolva.
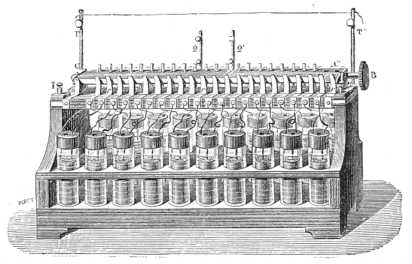
197. ábra. – Planté-féle másodrendű telep.
Ha a telepet tölteni akarjuk, az elemeknek nagy felületre kell összekapcsolva lenniök, úgy hogy a BUNSEN-féle oszlop, – e czélra mindig csakis két elemből összeállítva, – más ellenállásra ne akadjon, mint az
269
egyetlenegy elemnek tétlen elektromindító erejére, mely elemnek felülete 20-szor akkorává tétetett. A 198-ik magyarázó ábra, melyen mindegyik elem P1P2, P3P4.... két-két lemez által van előtüntetve, a kapcsolat ezen első módját jelzi: az összes páratlan sorszámú P1 P3... lemezek egymással közlekednek és negativ elektromosságot vesznek fel; ugyanoly módon a páros sorszamu lemezek mind positivokká lesznek.